 H2o2 mno2. Mn h2 h2o mn. Mn(oh)2+ o2. Mn3o4 h2 mno h2o тип. Mn2o7 кислотный.
H2o2 mno2. Mn h2 h2o mn. Mn(oh)2+ o2. Mn3o4 h2 mno h2o тип. Mn2o7 кислотный.
|
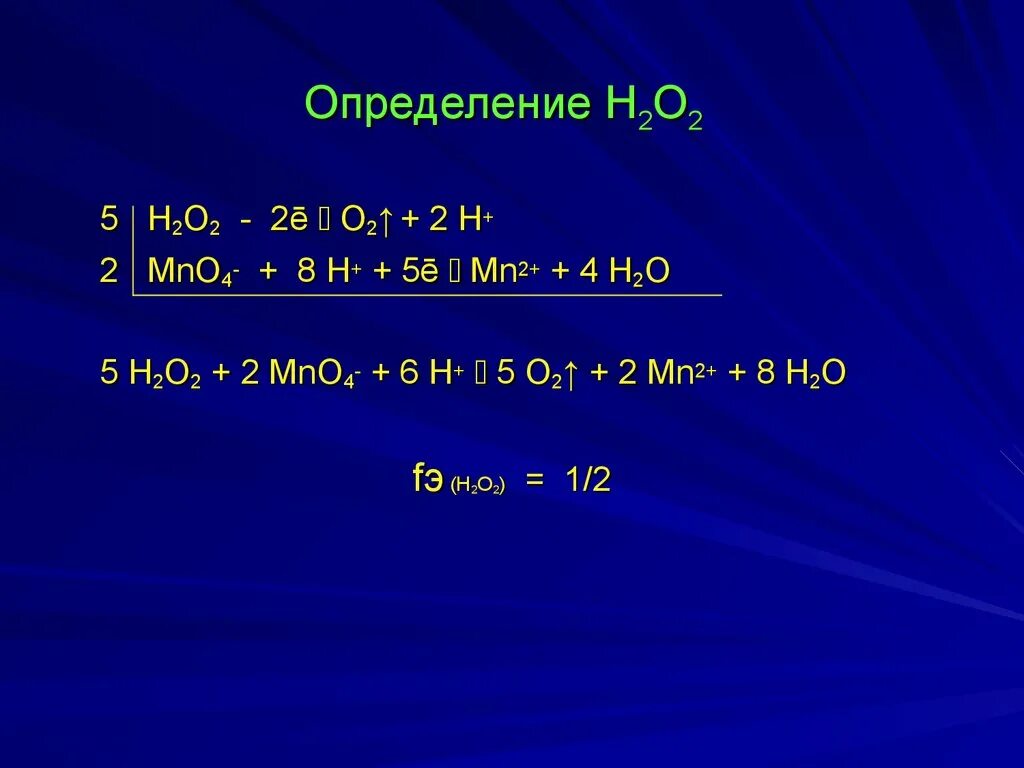 Ch3 ch2 ch ch2 kmno4 h2so4 овр. H2o2 mn02. Mn+h2o. H2o2 mn02. Mn h2 h2o mn.
Ch3 ch2 ch ch2 kmno4 h2so4 овр. H2o2 mn02. Mn+h2o. H2o2 mn02. Mn h2 h2o mn.
|
 Ch2 ch ch ch2 kmno4 h2so4 овр. Ионно-электронный метод. Mn02 mn2+. Mn+h2so4 концентрированная. Mn h2 h2o mn.
Ch2 ch ch ch2 kmno4 h2so4 овр. Ионно-электронный метод. Mn02 mn2+. Mn+h2so4 концентрированная. Mn h2 h2o mn.
|
 Mno2+ h2 - mn+h2o. Mn h2 h2o mn. Mno2+h2. H2o2 mn02. Mno2 овр.
Mno2+ h2 - mn+h2o. Mn h2 h2o mn. Mno2+h2. H2o2 mn02. Mno2 овр.
|
 Mn окисление. Н2о2+mno2. Mno2 h2 mn h2o. Mno2 hcl конц. Mn+h2o уравнение.
Mn окисление. Н2о2+mno2. Mno2 h2 mn h2o. Mno2 hcl конц. Mn+h2o уравнение.
|
 Mn h2 h2o mn. Mn oh 2 o2. Mn+h2o. C2h2 c2h4. Mn2o7 h2o уравнение.
Mn h2 h2o mn. Mn oh 2 o2. Mn+h2o. C2h2 c2h4. Mn2o7 h2o уравнение.
|
 С2н2+о2. H2o2 mn02. Mn oh 2 получение. Mno2+ h2 - mn+h2o. Mno+h2o.
С2н2+о2. H2o2 mn02. Mn oh 2 получение. Mno2+ h2 - mn+h2o. Mno+h2o.
|
 Mno2 h2o. Mno2 mn. Mn+h2o. Mn+h2o уравнение. Mno4 2- mno2 + mno4.
Mno2 h2o. Mno2 mn. Mn+h2o. Mn+h2o уравнение. Mno4 2- mno2 + mno4.
|
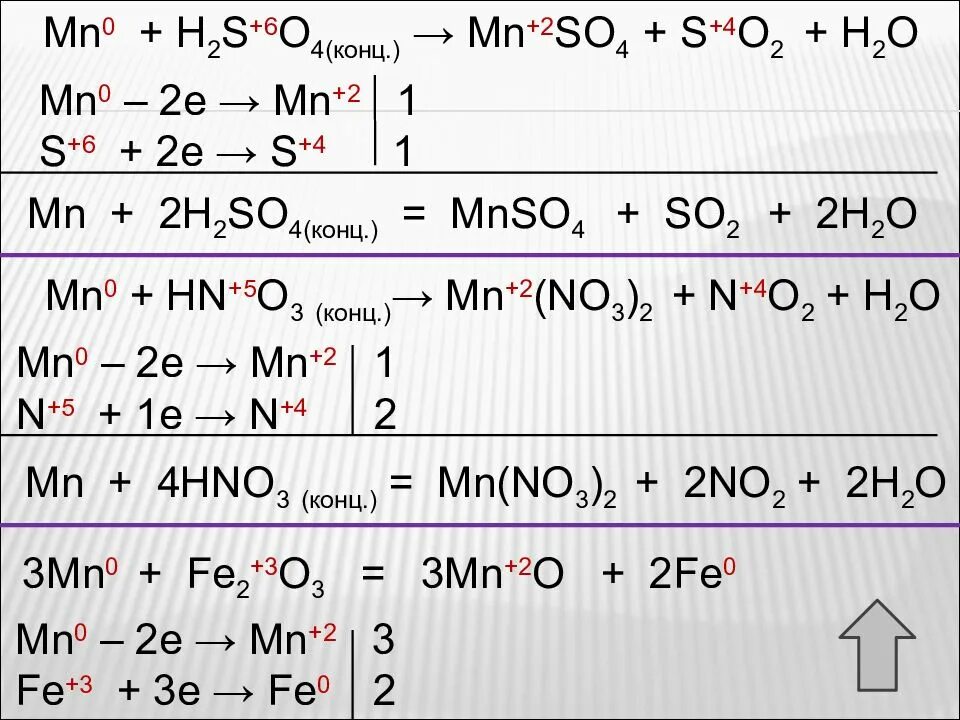 H2o2 mno2 овр. Перманганатометрия. H2o2 mno2. Mn2 2 oh- mn (oh)2. Из mno2 mn.
H2o2 mno2 овр. Перманганатометрия. H2o2 mno2. Mn2 2 oh- mn (oh)2. Из mno2 mn.
|
.PNG) H2+o2 окислительно восстановительная реакция. Разложение h2o2 в присутствии mno2. Mn(oh)3 = mn + h2o. Mn h2 h2o mn. Взаимодействие с основными и амфотерными оксидами серная кислота.
H2+o2 окислительно восстановительная реакция. Разложение h2o2 в присутствии mno2. Mn(oh)3 = mn + h2o. Mn h2 h2o mn. Взаимодействие с основными и амфотерными оксидами серная кислота.
|
 Mn h2 h2o mn. H2o2 mno2. Mno2 co. Mn h2 h2o mn. Mn+h2so4.
Mn h2 h2o mn. H2o2 mno2. Mno2 co. Mn h2 h2o mn. Mn+h2so4.
|
 Mn oh 2 mno2. Mn h2 h2o mn. Mn h2 h2o mn. Mn h2 h2o mn. Ch3 ch ch3 ch2 ch3 kmno4 h2so4.
Mn oh 2 mno2. Mn h2 h2o mn. Mn h2 h2o mn. Mn h2 h2o mn. Ch3 ch ch3 ch2 ch3 kmno4 h2so4.
|
 Mno2 h2 mn h2o. Mn h2 h2o mn. Mn h2so4 разб. Mn h2 h2o mn. Mn oh 2 разложение.
Mno2 h2 mn h2o. Mn h2 h2o mn. Mn h2so4 разб. Mn h2 h2o mn. Mn oh 2 разложение.
|
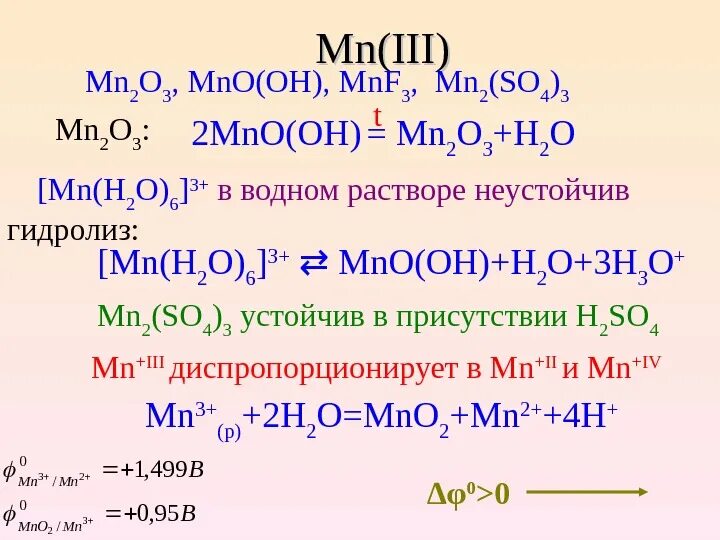 2н2о2 = 2н2о + о2. Mn2o3 h2. H202+mno2. Mno2+ h2 - mn+h2o. Mn h2 h2o mn.
2н2о2 = 2н2о + о2. Mn2o3 h2. H202+mno2. Mno2+ h2 - mn+h2o. Mn h2 h2o mn.
|
 Mn02h2. Mn h2 h2o mn. H2+mno2 уравнение реакции. Mn h2 h2o mn. H2o2 mn02.
Mn02h2. Mn h2 h2o mn. H2+mno2 уравнение реакции. Mn h2 h2o mn. H2o2 mn02.
|
 H2o2 mno2 уравнение. Mn окисление. Mn h2 h2o mn. Mn+h2. Mn h2so4 конц.
H2o2 mno2 уравнение. Mn окисление. Mn h2 h2o mn. Mn+h2. Mn h2so4 конц.
|
 Mn h2 h2o mn. Mn+o2 mn02. Mno2 h2 mn h2o. H2o2 катализатор mno2 уравнение. Mno4 в mno4 2-.
Mn h2 h2o mn. Mn+o2 mn02. Mno2 h2 mn h2o. H2o2 катализатор mno2 уравнение. Mno4 в mno4 2-.
|
 Mn h2 h2o mn. Mno+h2o. Mno mn2o3. Mn(oh)2+h2o. H2o2 mn02.
Mn h2 h2o mn. Mno+h2o. Mno mn2o3. Mn(oh)2+h2o. H2o2 mn02.
|
 Mno2 → mn2+. Mn h2 h2o mn. Mn+h2o уравнение. Mno2 h2o. Mn+h2o уравнение.
Mno2 → mn2+. Mn h2 h2o mn. Mn+h2o уравнение. Mno2 h2o. Mn+h2o уравнение.
|
 Mno4 2- mno2 + mno4. Mn h2 h2o mn. Mn02 mn2+. Mn2o7 кислотный. Mn h2 h2o mn.
Mno4 2- mno2 + mno4. Mn h2 h2o mn. Mn02 mn2+. Mn2o7 кислотный. Mn h2 h2o mn.
|
.PNG)

.PNG)
